9. Februar 2021, 19:57 Uhr | Lesezeit: 5 Minuten
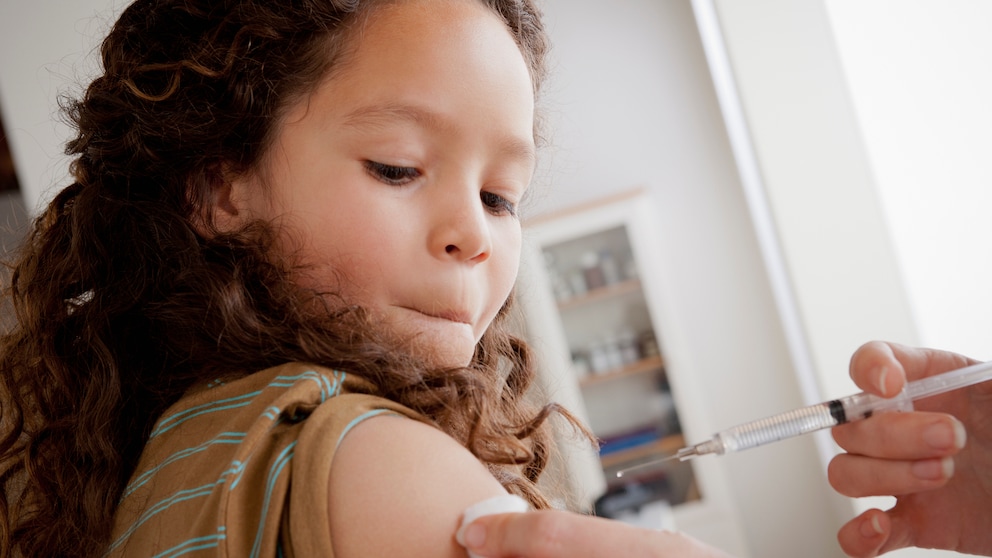
Wenn sich Kinder mit dem Coronavirus infizieren, sind schwere Verläufe selten. Dennoch werden auch für sie Impfstoffe entwickelt – um Erwachsene zu schützen. Das wirft Fragen auf.
Bisher werden die Ältesten gegen Covid-19 geimpft, aber bald soll es altersmäßig rückwärts gehen. Doch was ist mit der Corona-Impfung für Kinder? Ein einziger Impfstoff ist bisher ab 16 zugelassen, alle anderen nur für Erwachsene. Erst wenige Hersteller haben mit Studien an Minderjährigen begonnen. Denn das ist aufwendig: Je jünger Kinder werden, desto mehr.
Die Problematik bei Corona-Impfungen für Kinder
Fred Zepp rechnet „frühestens Ende des Jahres, eher Anfang nächsten Jahres damit“, dass Kinder in Deutschland geimpft werden könnten. „Der Prüfaufwand ist viel höher als bei Erwachsenen“, sagt der Direktor des Zentrums für Kinder- und Jugendmedizin der Universität Mainz, der Mitglied der Ständigen Impfkommission (Stiko) ist. „Je jünger der Mensch ist, desto ausgeprägter kann er reagieren und desto stärker sind eventuell auch Nebenwirkungen.“
„Vor der klinischen Prüfung an Kindern muss sichergestellt sein, dass in den Studien bei Erwachsenen keine schwerwiegenden Nebenwirkungen aufgetreten sind“, heißt es beim Robert Koch-Institut (RKI). „Kinder sind schon allein aus ethischen Gründen nicht für frühe Tests vorgesehen.“
Auch interessant: BioNTech, Moderna, J&J und AstraZeneca – vierCorona-Impfstoffe im Vergleich
Wie steht es bei der Entwicklung von Corona-Impfstoffen für Kinder?
Der Verband Forschender Arzneimittelhersteller (vfa) hat den Stand bei den Impfstoffherstellern zusammengetragen:
- Die Bedingte Zulassung des Impfstoffs von BioNTech/Pfizer umfasst bereits heute Jugendliche ab 16 Jahre. Im Herbst 2020 fügte das Duo laut vfa noch zwei Studienarme mit Teilnehmern von 12 bis unter 16 Jahren zur Studie hinzu: einen mit der echten Impfung und einen mit der Scheinimpfung. In der Planung ist es, auch Kinder zwischen 0 und 15 Jahren zu testen.
- Moderna hat bereits im Dezember damit begonnen, minderjährige Probanden zu suchen. Teilnehmen sollen nach Unternehmensangaben 3000 Kinder zwischen 12 und 17 Jahren. Bisher sind nur US-Kliniken an der „TeenCove“-Studie beteiligt. Zwei Drittel der Teilnehmer bekommen den Impfstoff, der Rest ein Placebo. Die Jugendlichen werden im Abstand von einem Monat zwei Mal geimpft und werden danach 13 Monate lang begleitet. Mindestens sechs Mal müssen sie in die Klinik, dazu kommen Telefonate und Rückmeldungen per App. Erwarteter Abschluss der Studie: Mitte 2022.
- AstraZeneca hat noch nicht mit pädiatrischen Studien begonnen. Man plane aber, „die Studien in einem neuen Protokoll für die Altersgruppe der 6- bis 18-Jährigen fortzusetzen“, heißt es bei dem britisch-schwedischen Hersteller. „Diese sollen in den kommenden Monaten beginnen.“ Details würden „zu gegebener Zeit“ bekannt gegeben. Bei diesem Impfstoff, den das Unternehmen mit der britischen Universität Oxford entwickelt hat, einem aus Indien und mehreren chinesischen wurden laut vfa Minderjährige bereits frühzeitig in Studien einbezogen. Die Studien sind zum Teil aber nicht abgeschlossen und fast alle Produkte in Europa gar nicht zugelassen.
Auch interessant: Wie hoch ist das Risiko bei derart schnell entwickelten Corona-Impfstoffen?
Ergebnisse von Studien mit Kindern unter 12 Jahren bis Ende 2024
Studien mit Kindern unter 12 Jahren gehören laut vfa sowohl für BioNTech/Pfizer als auch für Moderna zu den Auflagen der EMA, die an die „Bedingte Zulassungen für Erwachsene“ geknüpft sind. Spätester Abgabetermin der Ergebnisse sei Juli beziehungsweise Dezember 2024.
„Es ist zu erwarten, dass Studien mit diesen Altersgruppen nicht beginnen, ehe es nicht gute Ergebnisse zur Wirksamkeit und Verträglichkeit einer Impfung von Jugendlichen gibt“, heißt es in einem vfa-Papier. Üblicherweise arbeiten sich die Hersteller altersgruppenweise zu immer jüngeren Kindern vor. Jugendliche bekommen die gleiche Dosis wie Erwachsene. Bei jüngeren Kindern ist es möglich, dass die Dosis angepasst werden muss.
Das Paul-Ehrlich-Institut, das für die Sicherheit von Impfstoffen zuständig ist, betont: Impfstoffe werden nur für die Altersgruppen zugelassen, für die Daten zur Wirksamkeit und Sicherheit aus klinischen Prüfungen vorliegen. Die Zulassung würde dann durch eine sogenannte Änderungsanzeige zur bestehenden Zulassung auf Jüngere ausgedehnt.
Auch interessant: Was ist ein mRNA-Impfstoff – und verändert er mein Erbgut?
EU-Behörde gibt Empfehlung Weg frei für Moderna-Impfstoff für Kinder und Jugendliche
In der EU BioNTech beantragt Zulassung von Impfstoff für Kinder ab 12 Jahren
Corona EMA gibt BioNTech-Impfstoff für Kinder ab fünf Jahren frei
Noch keine Empfehlung zur Corona-Impfung für Kinder
Aber selbst wenn Produkte verfügbar sind, heißt das noch nicht, dass sie eingesetzt werden, und Kinder die Corona-Impfung erhalten. Auf die Frage „Wird es eine Impfempfehlung für Kinder gegen Covid-19 geben?“, antwortete das Robert Koch-Institut Anfang Januar: „Das ist bisher noch nicht absehbar.“
Kinder gegen Covid-19 zu impfen, sei zunächst einmal „fremdnützig“, sagt Kinderarzt Zepp. „Kinder erkranken dramatisch seltener schwerwiegend als Erwachsene. Wir würden Kinder also vor allem impfen, um Ältere zu schützen. Da müssen wir uns schon fragen, ob das abgesehen von Kindern mit besonderen Infektionsrisiken ethisch vertretbar ist.“
Und wenn man Kinder außen vor ließe: Wäre dann die angestrebte Herdenimmunität überhaupt zu erreichen? „Grundsätzlich ja“, sagt Zepp. Sie trügen zur Durchseuchung der Bevölkerung auch auf andere Weise bei: indem sie sich infizieren.
mit Material von dpa